2月27日发表在《细胞干细胞》上的一项研究表明,西奈山的研究人员发现了一种增强造血干细胞效力的方法,这可能为新的骨髓移植方法打开了大门。
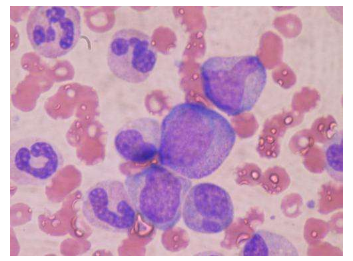
的稀缺性血 -形成干细胞,被称为造血干细胞(HSC),严重地限制了骨髓移植,它可以治愈许多血液疾病和实体瘤。西奈山研究小组报告说,操纵溶酶体周围的代谢活性,细胞内的储存和循环中心,可以使造血干细胞在骨髓移植中的功效提高90倍以上。
“造血干细胞一旦在培养皿中培养,就会失去干细胞潜能,这限制了它们在实验室中易于繁殖的能力,”医学发展与再生生物学教授医学博士Saghi Ghaffari说在西奈山伊坎医学院的黑人家庭干细胞研究所和蒂施癌症研究所任职,并担任这项研究的首席研究员。“为了使这些干细胞保持最佳效能,它们不应不断分裂-使其处于可改变其健康状况和寿命的代谢压力下。相反,它们应处于休眠或静止状态。但应保持静止体外血液干细胞的研究一直很困难,我们发现溶酶体是这些细胞休眠的关键。治疗价值。”
通过在小鼠中广泛的体内工作,西奈山的科学家使用了有效而又特异的溶酶体抑制剂,可降低溶酶体的酸度和细胞中氨基酸的释放。最终结果是将具有活化溶酶体的干细胞恢复到静止状态。这项研究进一步发现,抑制糖酵解作用(通过酶分解葡萄糖和其他糖类)还可以增强造血干细胞的静止性和效力,据信造血干细胞的能量依赖于糖酵解。
多年来,科学家一直在尝试在实验室中产生更多的HSC,以用于临床。干细胞生物学家,血液病公认专家Ghaffari博士解释说:“我们的方法与其他方法不同,因为它基于质量而不是数量。” “通过抑制溶酶体的活性,我们生产出的用于骨髓移植的造血干细胞数量减少了,但它们的作用要好得多,因为我们保留并增强了它们的效力。”
这项工作可用于从培养的多能干细胞(可以转变为任何类型的成熟细胞的主细胞)生成血液干细胞,或增强人类血液干细胞在骨髓移植中的功能,这是正在尝试的在Ghaffari博士的实验室中。它还引起了关于溶酶体对干细胞静止和效力的贡献及其潜在治疗应用的许多新问题。她实验室工作的另一个影响可能是识别和靶向传播包括白血病在内的血液恶性肿瘤的干细胞。